精准医学时代免疫微环境分子分型及免疫治疗耐(2)
尽管该分型实现了免疫细胞及分子层面的进一步细化,但仍然存在一些问题迫切需要解决:第一,PD-L1蛋白表达的时间、空间的抑制性以及各个公司采用的抗体并不一致,导致目前PD-L1检测存在分歧。例如,Pembrolizumab采用22C3伴随检测抗体,Nivolumab采用28-8作为伴随检测抗体,Atezolizumab采用SP142作为伴随检测抗体,而Durvalumab采用SP263作为伴随检测抗体,临床上各种针对PD-L1检测的解读铺天盖地,非肿瘤专科医生往往很难甄别,目前在肺癌领域,正在发起多中心的病理协作,制定以及比对各个抗体之间的特异性以及敏感性差异,解决临床现今检测的瓶颈;第二,针对TIL细胞的分类需要进一步细化,而不同类型的TIL浸润对预后指导意义大不相同;第三,针对TIL的计数评分常采用主观的二级半定量评分,可重复性不高,不同中心、不同病理师的阅片判读结果不容易达成一致;第四,常规方法难以满足肿瘤微环境分析的要求,如:蛋白印记和流式细胞学的方法丢失了肿瘤的形态信息;分子水平的检测(一代、二代测序、qPCR)能够分辨出足够多的基因型或细胞型组分,但无法判断这些组分在组织原位的空间位置关系,而这种定位关系对理解其在微环境中的作用又是至关重要的;常规免疫组化方法无法分辨足够多的细胞表型。综合以上,目前迫切需要开发出针对肿瘤微环境的多分子标记景观分析系统,同时建立每个分子的标准化检测流程,满足目前临床对免疫微环境的关键分子标记物需要定位、定量、定性分析的需求,同时还必须满足可重复性。例如,目前人工智能在数字化病理上探索应用,以及目前免疫评分体系在肠癌、肺癌以及乳腺癌的初步建立,都是对目前肿瘤免疫微环境分型的一个极大推动。
2、原发耐药的机制探索。免疫治疗原发耐药包含肿瘤细胞本身固有因素以及肿瘤细胞外部因素。固有因素包括:异常基因突变频率及总突变负荷;肿瘤抗原表达的缺失;原癌基因活化(EGFR、KRAS、MAPK,PI3K、WNT等)导致PD-L1的固有表达;肿瘤本身缺乏有效的抗原呈递系统;肿瘤本身缺乏主要组织相容性复合体(MHC)的表达;IFN-γ信号途径的异常突变导致肿瘤对杀伤性T细胞的不敏感等(见图1)。而外部因素包括:肿瘤微环境中缺乏杀伤性T细胞浸润; CTLA-4和其他免疫检查点的异常活化;T细胞衰竭和表型变化;免疫抑制性细胞群(Treg,MDSC,II型巨噬细胞)以及肿瘤微环境中细胞因子和代谢产物释放(CSF-1,色氨酸代谢物 ,TGF-β,腺苷)对免疫微环境产生的抑制效应(见图2)。
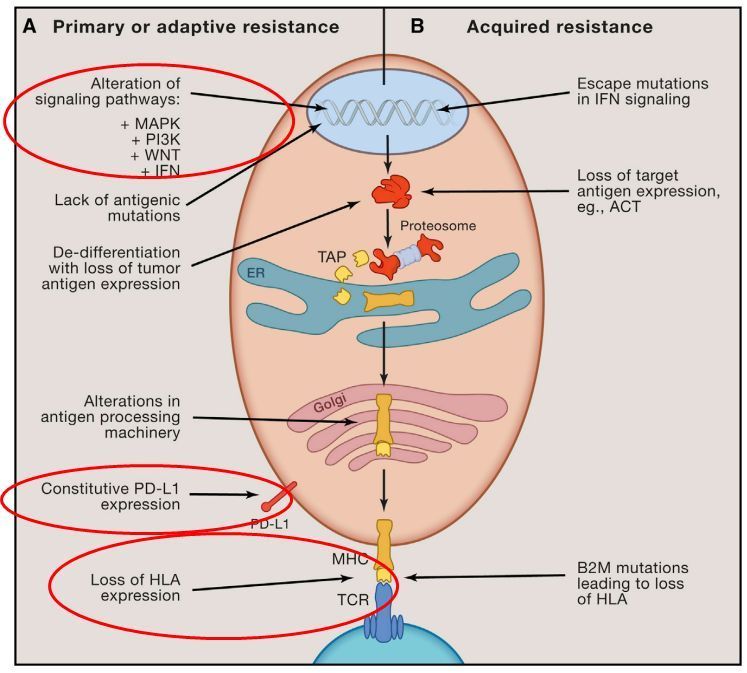
图1 肿瘤细胞对PD-1/PD-L1单抗治疗原发耐药及继发耐药的机制(引用自Padmanee Sharma,CELL,2017)

图 2 肿瘤细胞对PD-1/PD-L1单抗治疗耐药的外部因素(引用自Padmanee Sharma,CELL,2017)
对于上述复杂过程,如何发现、干预并深入挖掘其机制,是现阶段巨大的挑战。需要基础医学、转化医学以及临床医生的深入合作探索。通常目前认为,免疫治疗各个环节的多策略联合治疗是逆转耐药的有效方法,如化疗、放疗与PD-1/PD-L1抑制剂的联合使用,特别是局部放射治疗逆转耐药目前已经有诸多研究报道;肿瘤新抗原疫苗不仅可以协同PD-1/PD-L1增效,同时有逆转其耐药的理论基础;不同免疫检查点抑制剂的联合治疗,比如CTLA-4联合PD-1/PD-L1抑制剂,目前已有成熟的报道,而IDO抑制剂、OX40激动剂等正在进行临床研究;抗血管生成联合免疫治疗也有大量的临床研究正在开展;另外从机制上看,胸腺法新可以增强肿瘤抗原提呈作用,同时还可以促进肿瘤细胞表面MHC的表达,从而增强T细胞对肿瘤细胞的识别,改变肿瘤微环境,从而在一定程度上逆转耐药。有临床前的动物模型研究表明,PD-1抗体联合胸腺法新对荷瘤小鼠肝细胞癌皮下移植瘤有一定的协同作用,胸腺法新可能增强PD-1抗体的肿瘤抑制作用。
此外,对肿瘤、血液及其他样品采取基线和动态分析模式,可以帮助我们为现阶段及今后的深入研究作好准备。肿瘤微环境的基线评估通常包含对血液或组织样本的总突变负荷、驱动基因突变情况以及多基因表达的综合分析,也包括对CD8+T细胞的PD-L1、TCR表达情况及克隆能力的分析。而在治疗前后(治疗前、治疗早期和进展时间点)对新鲜连续人类标本(肿瘤,血液,血清和微生物组)进行纵向动态评价,则有可能通过深度分析揭示治疗抗性的潜在机制(见图3)。这种基线和动态的分析方法超越了对静态时间点的常规分析,并能通过动态评估癌症应答寻找优异的预测性生物标志物。因此,它将成为临床及转化基础研究中,深入揭示免疫检查点抑制剂反应及耐药机制的重要手段。
文章来源:《精准医学杂志》 网址: http://www.jzyxzz.cn/zonghexinwen/2020/1103/334.html